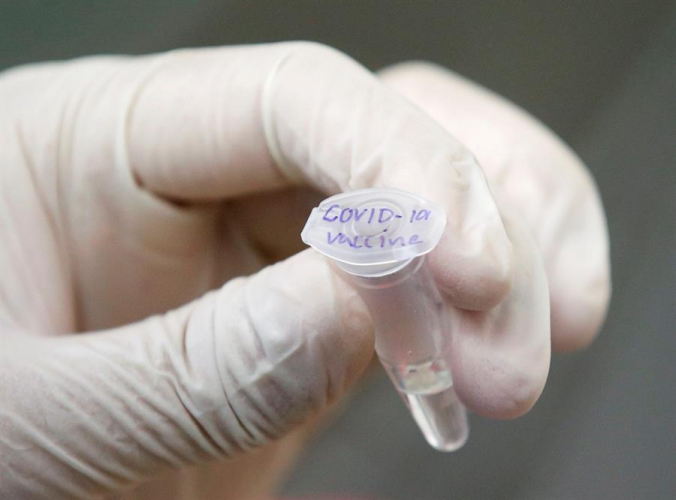
A farmacêutica AstraZeneca ainda está esperando aprovação da agência reguladora de remédios norte-americana para a retomada do teste clínico de sua possível vacina contra Covid-19. A espera de quase três semanas acontece após a testagem ser interrompida devido a preocupações de segurança. O teste norte-americano da vacina, desenvolvida inicialmente pela Universidade de Oxford, no Reino Unido, continua suspenso enquanto inspetores investigam uma doença em um dos participantes, mesmo depois de um estudo britânico e outros programas terem sido retomados fora dos Estados Unidos (EUA). “Somos os patrocinadores do estudo dos EUA. Por isso, providenciamos toda esta informação para a FDA (agência reguladora de medicamentos dos EUA) e estamos esperando para ouvir sua decisão”, disse Pascal Soriot, presidente-executivo da farmacêutica, em um debate virtual do Fórum Econômico Mundial. Alex Azar, secretário dos Serviços Humanos e de Saúde dos EUA, disse na quarta-feira, 23, que a manutenção da suspensão mostrou que a FDA está levando a segurança da vacina a sério.
Um documento publicado pela Universidade de Oxford disse que a doença em um participante britânico que provocou a interrupção no dia 6 de setembro pode não estar associada com a vacina. Indagado por que a empresa não revelou detalhes sobre a natureza da doença, Soriot disse que inspetores de testes clínicos e supervisores independentes estão preservando a privacidade dos participantes. “Estamos debatendo com outras empresas, como indústria, quais informações podemos oferecer sem comprometer a privacidade dos pacientes, mas também sem comprometer o próprio teste”, disse. Soriot ainda disse que os testes do protótipo da vacina em crianças ainda não começaram. O teste britânico, que foi iniciado em maio e recrutou mais de 12 mil voluntários, terá crianças de 5 a 12 anos em um de cada 11 subgrupos.
*Com Agência Brasil
Compartilhe




